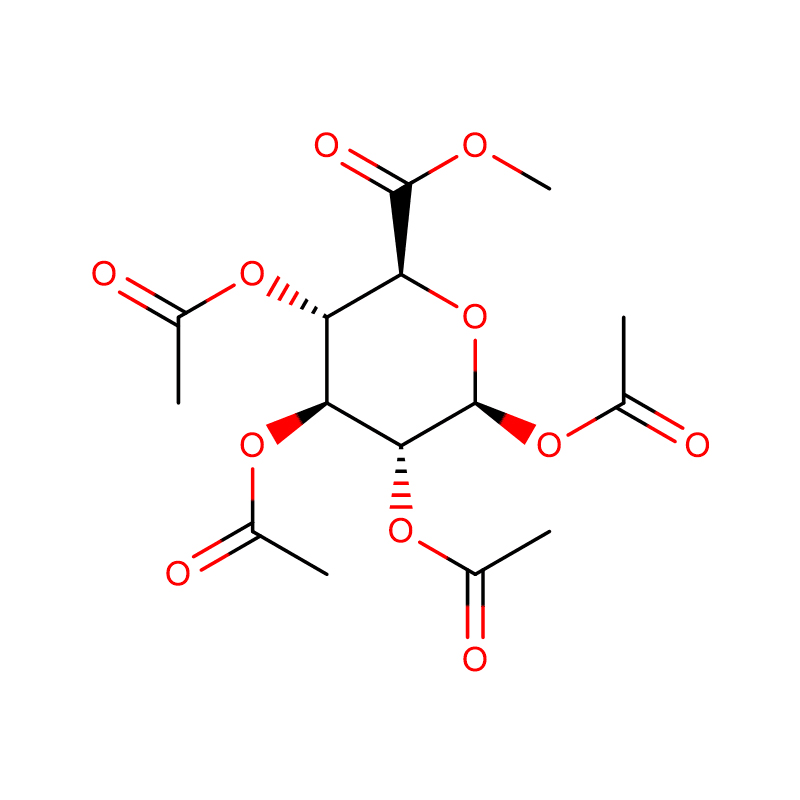
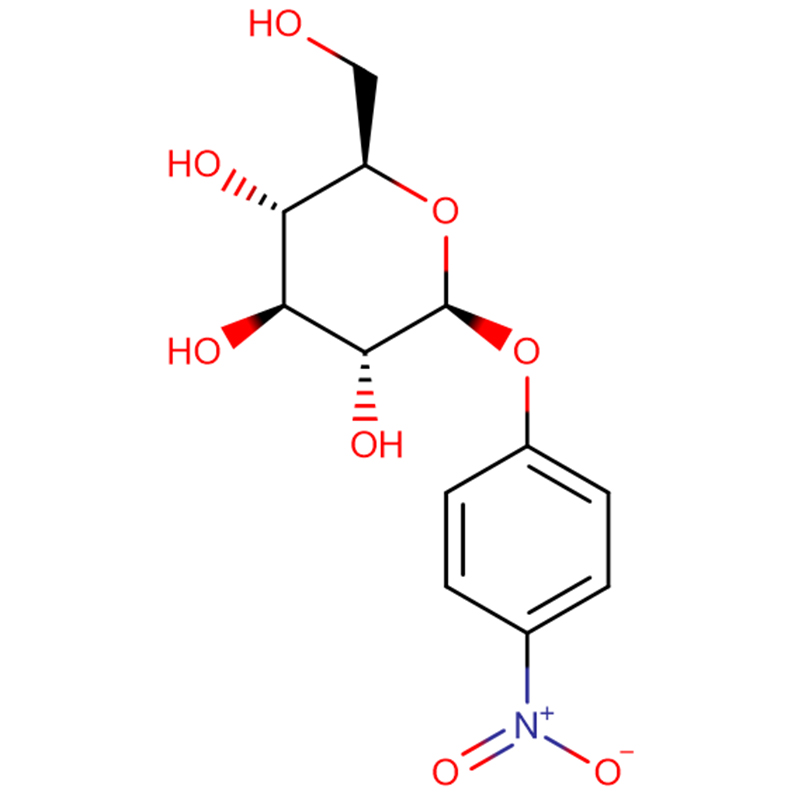
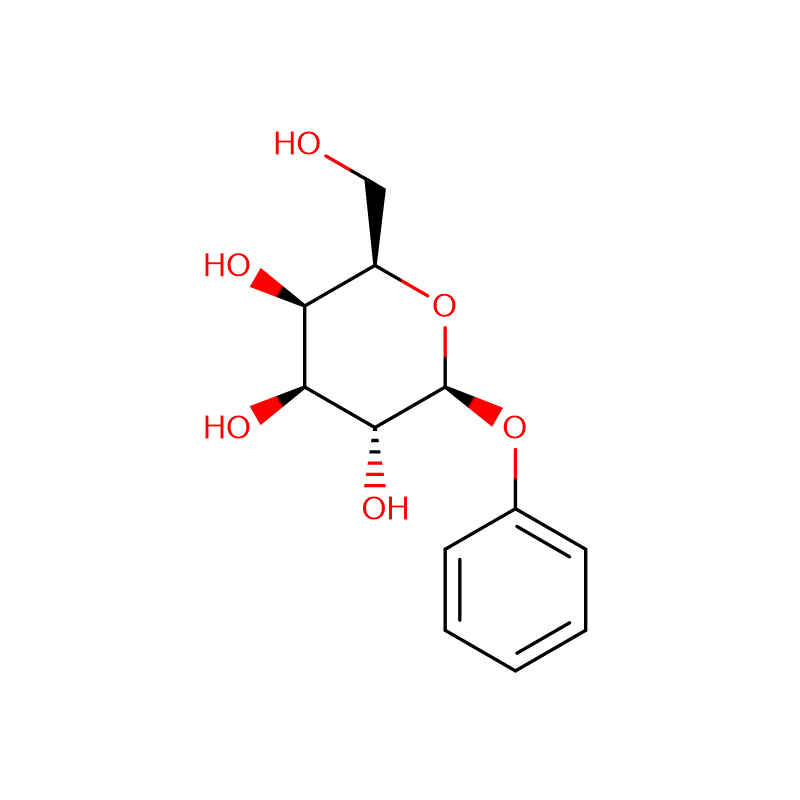
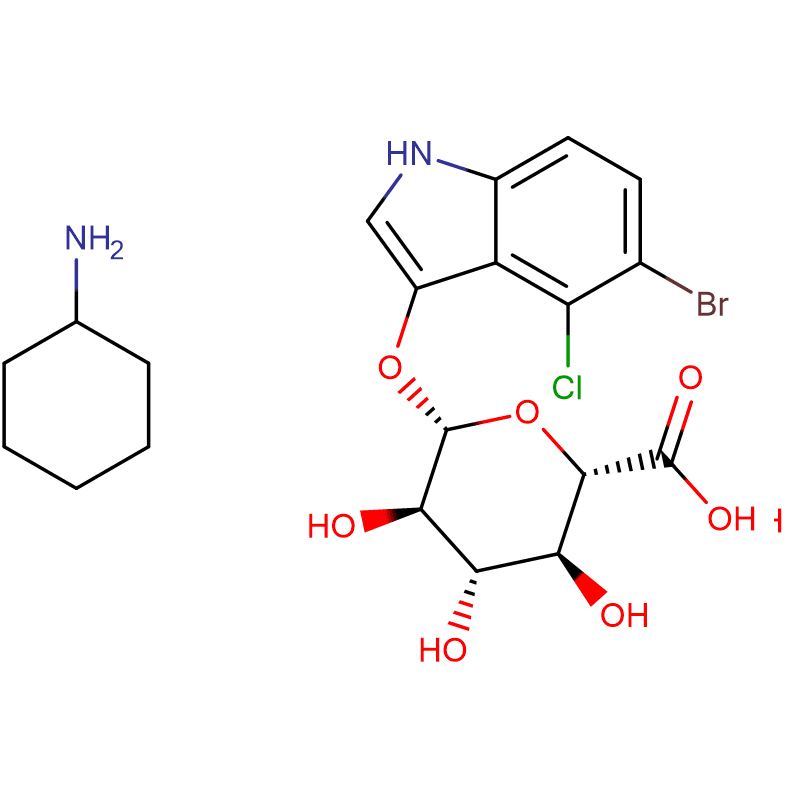
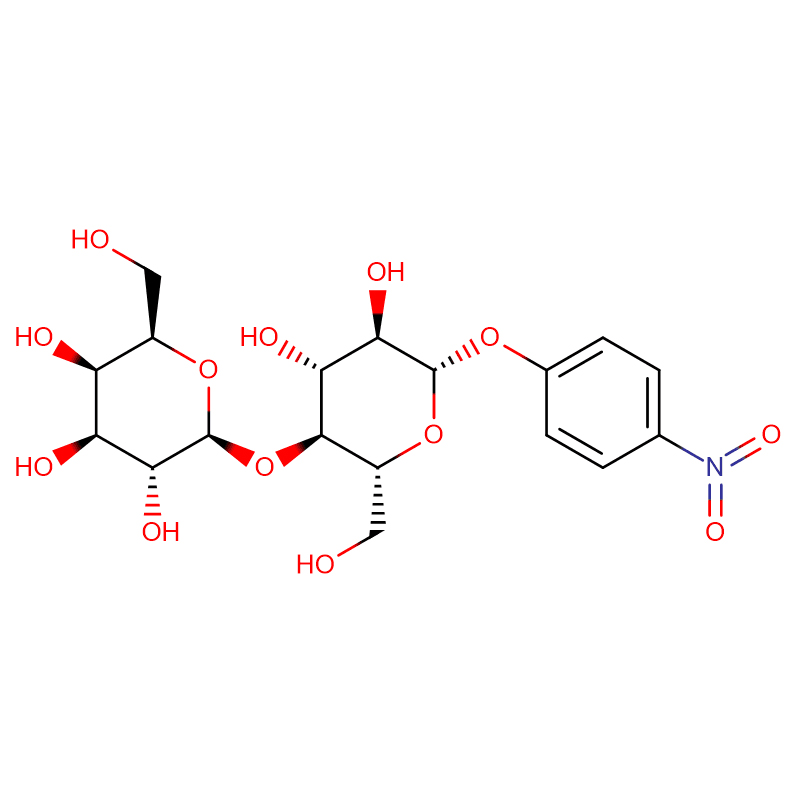
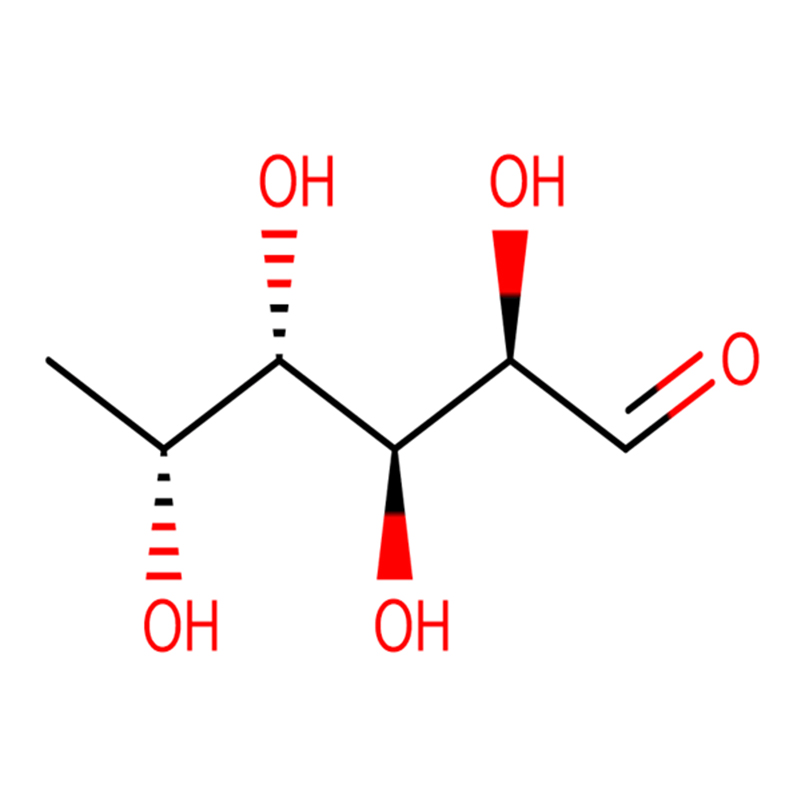
Dos anàlegs isomèrics de biciclo[4.1.0]heptà de l'inhibidor de la glicosidasa galacto-validamina, (1R*,2S,3S,4S,5S,6S*)-5-amino-1-(hidroximetil)biciclo[4.1.0]heptà -2,3,4-triol, s'han sintetitzat en 13 passos a partir de 2,3,4,6-tetra-O-benzil-D-galactosa.Les activitats inhibidores de les dues amines conformacionalment restringides, i les seves corresponents acetamides, es van mesurar contra enzims comercials alfa-galactosidasa del gra de cafè i E. coli.L'activitat de l'enzim GH27 de la família de la glicosil hidrolasa (gra de cafè) va ser inhibida competitivament per la 1R,6S-amina (7), una interacció d'unió que es va caracteritzar per un valor K (i) de 0,541 microM.L'alfa-galactosidasa d'E. coli GH36 va mostrar una interacció d'unió molt més feble amb la 1R,6S-amina (IC(50)= 80 microM).La 1S,6R-amina diastereomèrica (9) s'uneix feblement a les dues galactosidases, (gra de cafè, IC(50)= 286 microM) i (E. coli, IC(50)= 2,46 mM).